Profa. Dra. Karina Ramalho Bortoluci
 Título: Professora Associada – Departamento de Ciências Biológicas – UNIFESP
Título: Professora Associada – Departamento de Ciências Biológicas – UNIFESP
Laboratório: Laboratório de Imunologia Molecular
Local: Centro de Terapia Celular e Molecular – CTC-Mol, UNIFESP
Telefone: 55 (11) 50848807
E-mail: kbortoluci@gmail.com
Homepage: http://www.ctcmol.unifesp.br/<
lattes: lattes.cnpq.br/0159648961678651
Resumo:
O principal foco do nosso laboratório é o estudo de vias moleculares envolvidas na ativação dos inflamassomas e o seu impacto para o controle de infecções como Salmonella typhimurium, Trypanosoma cruzi e Zika virus
Linha de pesquisa:
1 – Mecanismos efetores mediados por inflamassomas
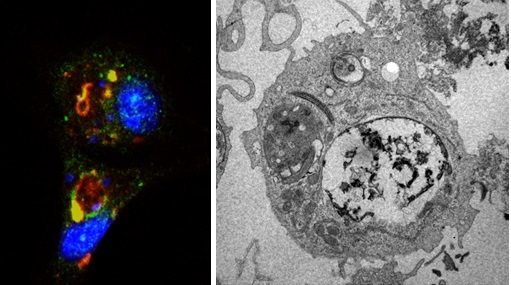
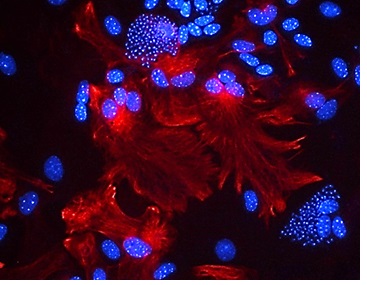
Os inflamassomas são complexos multiproteicos compostos por sensores citosólicos especializados para uma grande variedade de padrões moleculares de patógenos (PAMPs) ou danos celulares (DAMPs) e responsáveis pela ativação das caspase-1 com consequente secreção de IL-1b e IL-18 e indução de piroptose. Além desses mecanismos efetores canônicos, nosso grupo vêm estudando novos mecanismos mediados pelos inflamassomas, como ativação de processos microbicidas dos macrófagos, regulação epigenética de genes inflamatórios, ativação da resposta imune adaptativa e programas de morte da célula hospedeira.
2 – Interação entre inflamassomas e autofagia no controle da infecção pelo T. cruzi e Zika virus
A autofagia é um processo homeostático celular de reciclagem de organelas e nutrientes. Em processos infecciosos, a autofagia auxilia no controle de micro-organismos. Os receptores para padrões moleculares (PRRs) vêm sendo relacionados com a regulação de autofagia e controle de micro-organismos. Os receptores do tipo Toll (TLR) estão claramente envolvidos na ativação do processo autofágico. No entanto, o papel dos inflamassomas nesse processo ainda é bastante controverso. O objetivo dessa linha é verificar a influência dos inflamassomas na regulação da autofagia utilizando os modelos de infecção pelo T. cruzi e Zika vírus.
3 – Interação entre inflamassomas e necroptose no controle do T. cruzi e Zika virus
Além dos mecanismos microbicidas induzidos pelos PRRs, a necroptose, um tipo de morte celular regulada com fenótipo similar à necrose, vem sendo apontada como um mecanismo importante no controle de infecções ocasionadas por diversos patógenos. Estudos demostraram que na ausência de moléculas essenciais para a necroptose, como RIPK3, os animais se tornam mais susceptíveis a diversos tipos de infecção, tais como infecções virais e bacterianas. Além de induzir morte por necroptose, RIPK3 também está envolvido na ativação de respostas inflamatórias, incluindo aquelas mediadas por inflamassomas. Sendo assim, é possível que a via mediada por RIPK3 esteja envolvida na modulação da ativação dos inflamassomas. Sendo assim, a proposta central deste projeto é investigar o papel de RIPK3 tanto na indução da via de necroptose quanto na regulação da ativação dos inflamassomas e seu impacto para o controle das infecções por T. cruzi e Zika virus
4- Papel dos inflamassomas no sistema nervoso central (SNC)
Objetivo: Os inflamassomas, complexos multiproteicos responsáveis pela ativação da caspase-1, vêm sendo relacionados com o desenvolvimento de inúmeras patologias neurodegenerativas. O objetivo central dessa linha é entender a resposta diferencial de neurônios, microglias e astrócitos a ligantes clássicos de inflamassomas e o reflexo dessa ativação para o desenvolvimento de patologias inflamatórias e controle de infecções que atingem o SNC.
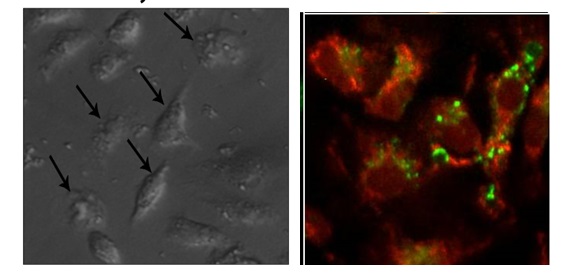
5 – Imunobiologia dos macrófagos
Os macrófagos, células residentes em tecidos distintos, representam uma população celular altamente heterogênea. A heterogeneidade dessas células está presente tanto em seus aspectos morfológicos e fenotípicos, como metabólicos e funcionais. Sendo assim, os macrófagos podem assumir papéis protetores ou deletérios ao hospedeiro. Nos últimos anos, muitas questões têm sido levantadas nesse tema, uma vez que além do microambiente, outros aspectos, que envolvem desde sua origem até seu estado de diferenciação, parecem igualmente refletir na heterogeneidade destas células. Desta forma, o objetivo central desta linha é elucidar os aspectos envolvidos na heterogeneidade dos macrófagos e verificar a capacidade diferencial dessas células no controle de infecções.
Autofagia em macrófagos
Piroptose e secreção de IL-1 por macrófagos
Infecção de células gliais do SNC
Principais publicações:
– Buzzo de Lima C, Medina T, Branco L, Lage S, Ferreira LCS, Amarante-Mendes GP, Hottiger M, Carvalho DD, Bortoluci KR. Epigenetic regulation of nitric oxide synthase 2, inducible (Nos2) by NLRC4 inflammasomes involves PARP1 cleavage. Scientific Reports, 7:41686, 2017.
-Ersching J, Basso AS, Calich VL, Bortoluci KR*, Rodrigues MM*. A Human Trypanosome Suppresses CD8+ T Cell Priming by Dendritic Cells through the Induction of Immune Regulatory CD4+ Foxp3+ T Cells. PLoS Pathog. 2016; 12(6):e1005698. doi: 10.1371/journal.ppat.1005698. eCollection 2016.*These authors share the sênior authorship
– Cassado A, D´império Lima MR, BORTOLUCI, KR. Revisiting Mouse Peritoneal Macrophages: Heterogeneity, Development, and Function. Frontiers in Immunology (Online), v. 6, p. 225, 2015.
– Lage SL, Longo C, Branco LM, da Costa TB, Buzzo Cde L, Bortoluci KR. Emerging Concepts about NAIP/NLRC4 Inflammasomes. Front Immunol. 2014 Jul 2;5:309. doi: 10.3389/fimmu.2014.00309. eCollection 2014.
– Amaral EP, Ribeiro SC, Lanes VR, Almeida FM, de Andrade MR, Bomfim CC, Salles EM, Bortoluci KR, Coutinho-Silva R, Hirata MH, Alvarez JM, Lasunskaia EB, D’Império-Lima MR. Pulmonary infection with hypervirulent Mycobacteria reveals a crucial role for the P2X7 receptor in aggressive forms of tuberculosis. PLoS Pathog. 2014 Jul 3;10(7):e1004188. doi: 10.1371/journal.ppat.1004188. eCollection 2014 Jul.
– Lage L, Amarante-Mendes G, BORTOLUCI KR. Evaluation of pyroptosis in macrophages using cytosolic delivery of purified flagellin. Methods 61(2):110-116; 2013.
– Gomes, MTR, Campos PC, Oliveira FS, Corsetti PP, BORTOLUCI KR. Cunha LD, Zamboni DS, Oliveira SC. Critical Role of ASC Inflammasomes and Bacterial Type IV Secretion System in Caspase-1 Activation and Host Innate Resistance to Brucella abortus Infection. The Journal of Immunology, 190(7): 3629-3638, 2013.
– Vasconcelos JR, Bruna-Romero O, Araújo AF, Dominguez MR, de Alencar BCG, Machado AV, Gazzinelli RT, BORTOLUCI KR, Amarante-Mendes GP, Lopes MF and Rodrigues MM. Pathogen-induced proapoptotic phenotype and high CD95 (Fas) expression accompany a suboptimal CD8+ T-cell response: Reversal by adenoviral vaccine. Plos Pathogen. PLoS Pathogens, 8(5):e1002699, 2012.
– Klionsky DJ, Abdalla FC, Abeliovich H, Abraham RT, Acevedo-Arozena A, Adeli K, Agholme L, Agnello M, Agostinis P, Aguirre-Ghiso JA, Ahn HJ, Ait-Mohamed O, Ait-Si-Ali S, Akematsu T, Akira S, Al-Younes HM, Al-Zeer MA, Albert ML, Albin RL, Alegre-Abarrategui J, Aleo MF, Alirezaei M, Almasan A, Almonte-Becerril M, Amano A, Amaravadi R, Amarnath S, Amer AO, Andrieu-Abadie N, Anantharam V, Ann DK, Anoopkumar-Dukie S, Aoki H, Apostolova N, Arancia G, Aris JP, Asanuma K, Asare NY, Ashida H, Askanas V, Askew DS, Auberger P, Baba M, Backues SK, Baehrecke EH, Bahr BA, Bai XY, Bailly Y, Baiocchi R, Baldini G, Balduini W, Ballabio A, Bamber BA, Bampton ET, Bánhegyi G, Bartholomew CR, Bassham DC, Bast RC Jr, Batoko H, Bay BH, Beau I, Béchet DM, Begley TJ, Behl C, Behrends C, Bekri S, Bellaire B, Bendall LJ, Benetti L, Berliocchi L, Bernardi H, Bernassola F, Besteiro S, Bhatia-Kissova I, Bi X, Biard-Piechaczyk M, Blum JS, Boise LH, Bonaldo P, Boone DL, Bornhauser BC, BORTOLUCI KR, Bossis I, Bost F, Bourquin JP………… Matarrese, P Guidelines for the use and interpretation of assays for monitoring autophagy. Autophagy, 8(4): 445-544, 2012. Fator de impacto JCR 2015: 9.108
– Lage SL, Buzzo CL, Amaral EP, Matteucci KC, Massis LM, Icimoto MY, Carmona AK, D’Império Lima MR, Rodrigues MM, Ferreira LC, Amarante-Mendes GP, Bortoluci KR. Cytosolic flagellin-induced lysosomal pathway regulates inflammasome-dependent and -independent macrophage responses. Proc Natl Acad Sci U S A. 2013 Aug 27;110(35):E3321-30. doi: 10.1073/pnas.1305316110.
– Gonçalves VM, Matteucci KC, Buzzo CL, Miollo BH, Ferrante D, Torrecilhas AC, Rodrigues MM, Alvarez JM, Bortoluci KR. NLRP3 controls Trypanosoma cruzi infection through a caspase-1-dependent IL-1R-independent NO production. PLoS Negl Trop Dis. 2013 Oct 3;7(10):e2469. doi: 10.1371/journal.pntd.0002469.
– Lima-Junior DS, Costa DL, Carregaro V, Cunha LD, Silva AL, Mineo TW, Gutierrez FR, Bellio M, Bortoluci KR, Flavell RA, Bozza MT, Silva JS, Zamboni DS. Inflammasome-derived IL-1β production induces nitric oxide-mediated resistance to Leishmania. Nat Med. 2013 Jul;19(7):909-15. doi: 10.1038/nm.3221.
– Cassado A, de Albuquerque JA, Sardinha LR, Buzzo C de L, Faustino L, Nascimento R, Ghosn EE, Lima MR, Alvarez JM, Bortoluci KR. Cellular renewal and improvement of local cell effector activity in peritoneal cavity in response to infectious stimuli. PLoS One. 6(7):e22141, 2011.
– Buzzo CL, Campopiano JC, Massis LM, Lage SL, Cassado AA, Leme-Souza R, Dias da Cunha L, Russo M, Zamboni DS, Amarante-Mendes GP, Bortoluci KR. A novel pathway for inducible nitric oxide synthase (iNOS) activation through inflammasomes. Journal of Biological Chemistry. 285(42):32087-95, 2010.
– Bortoluci KR, Medzhitov R. Control of infection by pyroptosis and autophagy: role of TLR and NLR. 2010. Cellular and Molecular Life Sciences. 67(10):1643-51, 2010.
– Ghosn EE, Cassado AA, Govoni GR, Fukuhara T, Yang Y, Monack DM, Bortoluci KR, Almeida SR, Herzenberg LA, Herzenberg LA. Two physically, functionally, and developmentally distinct peritoneal macrophage subsets. Proc Natl Acad Sci U S A. 107(6):2568-73, 2010.
Equipe:
Links:
http://www.researcherid.com/rid/C-6018-2012
http://scholar.google.com.br/citations?user=YBlW7FkAAAAJ&hl=pt-BR
https://orcid.org/0000-0001-6780-5397
http://loop.frontiersin.org/people/83403/overview
Grupo de pesquisa do CNPq:
Copyright © 2024 Programa de Pós-Graduação em Imunologia | Produzido por SCS - Mídias Online